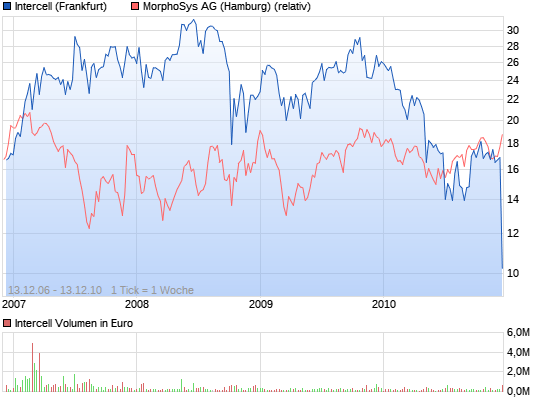
Intercell gekauft...
| eröffnet am: | 21.04.05 15:37 von: | börsenfüxlein |
| neuester Beitrag: | 29.05.13 20:25 von: | proxima |
| Anzahl Beiträge: | 577 | |
| Leser gesamt: | 163561 | |
| davon Heute: | 24 | |
bewertet mit 9 Sternen |
||
|
|
||
Zettlmeissl und Kandera kauften bei unter 15 Euro
Nachdem die Intercell-Aktie in der Vorwoche auf rund 14 Euro zurückgefallen ist, haben die Vorstände Gerd Zettlmeissl und Reinhard Kandera die Schwächephase für den Kauf von Aktien genutzt. Zettlmeissl legte sich 2000 Stück zu 14,54 Euro ins Depot, Kandera 1000 Aktien zu 14,69 Euro. (red
http://www.boerse-express.com/pages/892793
für mich sind das jetzt - in anbetracht der fundamentals und des chartbildes eindeutige kaufkurse.
mich würde es nach wie vor interessieren ob so "mittelständische" unternehmen in der branche auf lange sicht überhaupt die mittel haben um erfolgreich zu sein - oder ob es nicht fast schon ziel sein muss geschluckt zu werden - da man sich stand alone mässig nur aufreibt...
Allerdings ich bleibe mit erheblichem Teil long.
Spaß beiseite, jeder muss selber möglichts richtige Entscheidung treffen wobei wir kleine Anleger sehr oft als Kanonenfutter dienen.
siehe:
http://www.ariva.de/news/Novartis-steigert-Umsatz-und-Ergebnis-3479338
ich sag nur starke partner sind gut für weitere kooperationen oder auch für die aufstockung der beteiligung...
Schreibt das Unternehmen schon Gewinne???
DANKE für euere Antworten!
EANS-Adhoc: Intercell AG gibt Ergebnisse für das 3. Quartal 2010 und aktuellen Überblick über F&E-Fortschritte und Management-Team bekannt
07:38 09.11.10
Ad-hoc-Mitteilung übermittelt durch euro adhoc mit dem Ziel einer europaweiten Verbreitung. Für den Inhalt ist der Emittent verantwortlich.
--------------------------------------------------
9-Monatsbericht 09.11.2010 Positiver Umsatztrend beim Impfstoff gegen Japanische Enzephalitis, IXIARO®/JESPECT®, setzt sich fort - Gezielte F&E-Ausgaben für fortgeschrittene Programme und negative Währungseffekte führen zu einem Verlust von EUR 27,8 Mio. im 3. Quartal - Gute Fortschritte bei Programmen zur Impfstoffentwicklung Wien (Österreich), 9. November 2010 - Die Intercell AG (VSE: ICLL) veröffentlichte heute die Ergebnisse des 3. Quartals 2010 und berichtete über Forschungs- und Entwicklungsfortschritte sowie über Veränderungen im Vorstand des Unternehmens. Unternehmenszahlen im Überblick >> IXIARO und JESPECT Verkaufserlöse zeigen kontinuierliches Wachstum im Vergleich zum Vorjahr - Die Verkaufserlöse beliefen sich in den ersten neun Monaten des Jahres (bis 30. September 2010) auf insgesamt EUR 9,4 Mio., verglichen mit EUR 5,6 Mio. im selben Zeitraum des Vorjahrs. >> Die kumulierten Umsätze von Intercell sanken in den ersten neun Monaten des Geschäftsjahres gegenüber der Vergleichsperiode um 28,4 % von EUR 29,5 Mio. auf EUR 21,1 Mio. >> Der Nettoverlust stieg in den ersten neun Monaten des Jahres 2010 auf EUR 50,9 Mio., in erster Linie wegen höherer Aufwendungen für Forschung und Entwicklung für vorangeschrittene klinische Studien sowie wegen nicht- liquiditätswirksamer Währungseffekte. >> Starke Cash-Position von EUR 107,1 Mio. >> Ausblick für das Gesamtjahr 2010: Für das Geschäftsjahr 2010 wird ein Konzernverlust von etwa EUR 40,0 Mio. erwartet; dies liegt im oberen Bereich des bisher kommunizierten Gesamtjahresausblicks und setzt den positiven Ausgang von anstehenden Entwicklungs-Meilensteinen voraus. Finanzkennzahlen TEUR 3. Quartal 1. bis 3. Quartal Geschäftsjahr 2010 2009 2010 2009 2009 Umsatzerlöse 6.704 9.159 21.118 29.480 61.681 Periodenergebnis (27.844) (14.671) (50.892) (25.925) (18.375) Nettomittelabfluss aus der laufenden Geschäftstätigkeit (22.724) (14.753) (49.218) (43.322) (25.995) Barbestand, kurzfristige Guthaben u. handelbare Wertpapiere am Ende der Periode 107.141 139.746 107.141 139.746 180.019 IXIARO®/JESPECT® Intercell berichtet, dass der positive Umsatztrend von IXIARO/JESPECT im 2. Quartal 2010 im 3. Quartal fortgesetzt werden konnte. Der Impfstoff von Intercell ist der einzige in Europa zugelassene JE-Impfstoff. Das Vakzin wird für die USA, die EU und Kanada produziert und dort ausgeliefert. Die Verkäufe an das US-Militär hängen 2010 von der weiteren Verwendung der Restbestände an JE-Vax® ab. Im Jahr 2011 ist eine beträchtliche Umsatzsteigerung möglich, da erwartet wird, dass die Bestände an JE-Vax dann aufgebraucht sein werden bzw. nicht weiter verwendet werden. Das Gesundheitsministerium der Regierung der Sonderverwaltungszone Hongkong hat den Impfstoff von Intercell zur Prävention von Japanischer Enzephalitis zugelassen. Der Zulassungsprozess für weitere Gebiete wurde initiiert. Darüber hinaus werden weitere Empfehlungen für andere Schlüsselländer in Europa erwartet. Diese Impfempfehlungen sind wesentlich, um das Bewusstsein für das Produkt weiter zu stärken und dadurch ein entsprechendes Marktwachstum zu erzielen. Die pädiatrischen Phase III-Studien mit IXIARO/JESPECT zum Schutz von Kindern, die in endemische Gebiete reisen, verlaufen nach Plan. Daten werden 2012 erwartet. Diese Studien bilden die Grundlage für eine Label-Erweiterung, die dazu dient, den bestehenden Impfstoff für reisende Kinder zur Verfügung zu stellen. Auf Basis der Intercell-Technologie wird ein neuer JE-Impfstoffkandidat für endemische Märkte entwickelt. Die WHO empfiehlt für diese Gebiete eine Aufnahme der Impfung gegen Japanische Enzephalitis in die nationalen Impfprogramme. Die klinische Entwicklung in endemischen Gebieten verzeichnet Fortschritte: Für Ende 2010 / Anfang 2011 ist eine pivotale Phase III-Studie bei Kindern geplant, die von Biological E., einem Partner von Intercell, in Indien finanziert und durchgeführt wird. Führendes F&E Portfolio im Bereich der hospitalen Infektionen In einer klinischen Phase II-Studie mit dem Impfstoffkandidaten IC43 gegen Infektionen mit dem Bakterium Pseudomonas aeruginosa wurden die primären Endpunkte hinsichtlich Immunogenität und Sicherheit erreicht. Außerdem wurde ein signifikanter Rückgang der Mortalität bei jener Gruppe beobachtet, welcher der nicht-adjuvantierte Impfstoff verabreicht wurde (verglichen mit der Sterblichkeit in der Placebo-Gruppe). Wird dies durch eine pivotale klinische Studie belegt, so könnte IC43 zu einem bedeutenden Impfstoff für Patienten auf Intensivstationen werden. Diese Patienten sind einem besonders hohen Todesrisiko aufgrund hospitaler Infektionen ausgesetzt. Der Impfstoff rief eine gute Immunreaktion hervor und wurde von den Probanden gut vertragen. Ernsthafte Impfstoff-assoziierte Nebenwirkungen, die zu Sicherheitsbedenken führen würden, wurden nicht beobachtet. Diese Ergebnisse stellen eine gute Basis für die Bewertung der Weiterentwicklungsoptionen dar. Intercell und Partner Novartis werden die nächsten Schritte festlegen. Start der klinischen Entwicklung mit Clostridium difficile-Programm: Nach erfolgreichen präklinischen Studien entwickelt Intercell seinen Impfstoffkandidaten gegen Infektionen mit Clostridium difficile (C. diff) weiter. C. diff gilt in Europa und den USA als Hauptursache für hospitale Durchfallerkrankungen. Der Beginn einer klinischen Phase I-Studie wird im Jahr 2010 erwartet. Entwicklung des Impfstoffs gegen Staphylococcus aureus (V710) verläuft planmäßig: Die Phase II/III-Studie bei Kardiothorax-Patienten mit dem Impfstoffkandidaten zur Vorbeugung von S. aureus-Infektionen (finanziert und durchgeführt von Merck & Co.) verläuft nach Plan. Eine erste entscheidende Interimsanalyse (über die Machbarkeitsanalyse hinausgehend) wird für 2011 erwartet. Gute Fortschritte innerhalb der starken Entwicklungs-Pipeline - Programme verlaufen planmäßig >> Die Rekrutierung von etwa 2.000 Reisenden für die pivotale Phase III-Studie für das Impfpflaster gegen Reisedurchfall ist abgeschlossen. Erste Studienergebnisse von Reisenden nach Mexiko und Guatemala werden Ende 2010 / Anfang 2011 erwartet. Die Rekrutierung für eine ergänzende Phase II-Studie mit 800 Indienreisenden ist ebenfalls abgeschlossen; erste Daten werden für das 4. Quartal 2010 erwartet. Die Studie in Indien ist die erste Studie außerhalb von Südamerika und hat das Potenzial, den Nachweis für einen Proof- of-Konzept in Asien zu erbringen. >> Intercell wird die Aktivitäten zur Marktvorbereitung gemeinsam mit GSK fortführen, sobald die Daten der Phase II- und Phase III-Studien verfügbar sind. Durchfall ist das häufigste Gesundheitsproblem für Menschen, die aus Industrieländern in Entwicklungsländer reisen. Die meisten Fälle von Reisedurchfall werden durch Bakterien, in erster Linie ETEC-Stämme (Escherichia coli), hervorgerufen. >> Intercell und GSK werden die Entwicklung des Vaccine Enhancement Patch (VEP - immunstimulierendes Impfpflaster) gegen Vogelgrippe (H5N1) als Teil jener Kooperationsvereinbarung, die im Dezember 2009 unterzeichnet wurde, fortsetzen. Der Start einer entsprechenden klinischen Studie wird für Ende 2010 / Anfang 2011 erwartet. >> Intercell setzt die Zusammenarbeit mit GSK fort, um die Verwendung der Pflastertechnologie auf andere bestehende Impfstoffe auszuweiten. Management Seit dem 1. Oktober 2010 ist Staph Leavenworth Bakali Chief Business Officer und damit Mitglied des Vorstands von Intercell. Seine Hauptaufgaben liegen im Bereich der Kommerzialisierung. Bakali leitet die Bereiche Marketing & Sales, Corporate & Business Development sowie Alliance Management. Den gesamten Bericht finden Sie unter: http://www.intercell.com/de/ho me/forinvestors/downloads/quartalsberichte/ Ende der Mitteilung euro adhoc
http://www.ariva.de/news/...rgebnisse-fuer-das-3-Quartal-2010-3573681
12.12.2010 23:39
EANS-Adhoc: Intercell informiert über klinische Studien des Pflaster-Impfstoffs gegen Reisedurchfall
-------------------------------------------------- ------------ Ad-hoc-Mitteilung übermittelt durch euro adhoc mit dem Ziel einer europaweiten Verbreitung. Für den Inhalt ist der Emittent verantwortlich. -------------------------------------------------- ------------
12.12.2010
» Der Impfstoffkandidat gegen Reisedurchfall hat die Endpunkte (Schutz vor durch enterotoxische E. coli hervorgerufene Reisedurchfall-Infektionen; definiert als Fälle, in denen ETEC LT, LT/ST oder ST Toxine in Stuhlproben nachgewiesen werden können) in pivotalen, randomisierten und plazebo- kontrollierten Wirksamkeitsstudien (Phase II und Phase III) nicht erfüllt
» Dennoch legen die Studien die Weiterverfolgung der Pflaster-Technologie als geeignete Methode zur Immunisierung für zukünftige mögliche Impfstoffkandidaten nahe. Die pivotalen Studien bestätigen, dass der Impfstoffkandidat ein reproduzierbares Niveau an schützenden Antikörpern gegen das LT-Toxin induziert, was zu einer aussagekräftigen Reduktion von LT- spezifischen ETEC-Fällen nach transkutaner Immunisierung führte.
» Da das Unternehmen Meilensteinzahlungen im Zusammenhang mit dem Programm gegen Reisedurchfall voraussichtlich nicht erhalten wird und eine Wertberichtigung aller oder eines erheblichen Teils der entsprechenden immateriellen Anlagegüter erwartet, wird der geplante Verlust im Gesamtjahr 2010 erheblich höher als die bisher prognostizierten EUR 40 Mio. ausfallen
» Intercell hat beschlossen, die klinische Entwicklung des Impfpflasters gegen Reisedurchfall nicht weiter zu verfolgen
» Intercell wird die Ausgaben für Forschung und Entwicklung im Jahr 2011 um etwa 40 % im Vergleich zu 2010 reduzieren und die organisatorischen Strukturen entsprechend anpassen
» Der Vorstand wird die Forschungs- und Entwicklungsstrategie sowie die Ressourcen des Unternehmens auf die anderen Projekte des ausgewogenen Portfolios an Produktkandidaten in klinischer Entwicklung konzentrieren - insbesondere auf die erfolgreichen und hochattraktiven nosokomialen Programme - dazu zählen die Impfstoffkandidaten gegen Pseudomonas und C. difficile sowie ein Impfstoffkandidat gegen S. aureus, der mit Merck& Co., Inc. entwickelt wird. Der Vorstand wird außerdem den positiven Trend steigernder Produktverkäufe des Impfstoffs gegen Japanische Enzephalitis weiter vorantreiben
Wien (Österreich) / Gaithersburg (USA), 12. Dezember 2010 - Die Intercell AG (VSE: ICLL) gab heute die vorläufigen klinischen Ergebnisse des Impfpflasters gegen Reisedurchfall sowie die Entscheidung, die Entwicklung dieses Impfstoffkandidaten nicht weiter zu verfolgen, bekannt. Die Entscheidung beruht auf den neuesten Ergebnissen der randomisierten und plazebo-kontrollierten Phase III-Studie (ELT301), an der 2036 europäische Reisende nach Mexiko und Guatemala teilnahmen, sowie der Phase II-Pilotstudie zur Wirksamkeit (ELT209), an der 723 europäische Reisende nach Indien teilnahmen.
Beide Studien wurden erfolgreich entsprechend dem Studiendesign durchgeführt, erfüllten die statistischen Ziele zu Rekrutierung, Teilnehmer-Follow-up, Einwilligung der Probanden und Studienzentren und lieferten ein klares vorläufiges Ergebnis. Der Impfstoff erwies sich generell als gut verträglich und das Nebenwirkungsprofil entsprach dem in früheren Studien.
In einer früheren randomisierten plazebo-kontrollierten Phase II-Doppelblind-Feldstudie (ELT206) zeigte der Impfstoffkandidat gegen Reisedurchfall hervorragende Immunogenität und ein verringertes Risiko klinisch signifikanter Durchfallerkrankungen bei Reisenden aus den USA nach Mexiko und Guatemala. Die Phase III-Studie sollte die Wirksamkeit des Impfpflasters gegen Reisedurchfall im Hinblick auf mittlere bis schwerwiegende Durchfallerkrankungen (ausgelöst durch ETEC und alle anderen Ursachen) in einer ähnlichen Feldstudie bestätigen.
Die primären Endpunkte der Studie, nämlich eine Reduktion der Häufigkeit von Reisedurchfall durch alle Arten von enterotoxische E. coli (ETEC; definiert als Fälle, in denen ETEC LT, LT/ST oder ST Toxine in Stuhlproben nachgewiesen werden können) und/oder Reisedurchfall durch alle Ursachen (sekundäre Endpunkte), wurden nicht erfüllt. In der ELT301-Studie wurde eine nicht signifikante Wirksamkeit der Impfung von etwa 35 % für alle ETEC-Arten und kein sichtbarer Effekt auf die Häufigkeiten aller moderaten bis schweren Durchfallerkrankungen beobachtet. Dennoch wurde eine statistisch signifikante Reduktion der Dauer aller Durchfallerkrankungen und der Gesamtzahl ungeformter Stuhlgänge beobachtet, was die Beobachtungen aus einer früheren Phase II-Studie bestätigt.
In der ELT301-Studie schützte der Impfstoff vor allem vor LT-positivem ETEC (bis zu 60 %). Allerdings war die Studie nicht darauf ausgelegt, eine statistisch signifikante Wirksamkeit gegen individuelle Arten von ETEC nachzuweisen. Des Weiteren war die Häufigkeit von LT-positivem ETEC im Vergleich zu früheren Studien und publizierten Daten in beiden Studien geringer als erwartet.
Die aktuellen Studien haben die frühere Beobachtung aus Phase II-Studien, wonach sich nach einer transkutanen Immunisierung unter Verwendung der unternehmenseigenen Verabreichungstechnologie eine konsistente Induktion schützender Antikörper-Niveaus gegen das LT-Toxin zeigt, bestätigt. Dies stärkt und bestätigt die Eignung des Impfpflasters als Art der Immunisierung für zukünftige mögliche Produktkandidaten klar.
Intercell wird die Studienergebnisse noch im Detail analysieren. Dennoch bleibt das Unternehmen, vorbehaltlich weiterer Analysen und Rücksprachen mit seinem Partner, entschlossen die Entwicklung zur Anwendung der Pflaster-Technologie für neue oder bestehende Impfstoffe auszuweiten und die Entwicklung des immunstimulierenden Impfpflasters "Vaccine Enhancement Patch" (VEP) gegen die H5N1-Vogelgrippe voranzutreiben.
Angesichts der aussichtsreichen Fortschritte des Impfstoffkandidaten gegen S. aureus ? Intercell veröffentlichte dazu erst kürzlich von Partner Merck&Co., Inc. berichtete positive Phase II-Daten ? der viel versprechenden Phase II-Daten des Impfstoffprogramms gegen Pseudomonas und der bevorstehenden klinischen Phase I-Studie des neuen Impfstoffkandidaten gegen C. difficile werden die Ressourcen in Forschung und Entwicklung hinkünftig noch stärker auf die Entwicklung des nosokomialen Produktportfolios konzentriert. Krankenhausinfektionen stellen einen Bereich mit hohem medizinischen Bedarf dar - Intercell ist mit seinem Portfolio in einer guten Position, diesem Bedarf Rechnung zu tragen.
Immaterielle Anlagegüter, die dem Impfstoffprogramm gegen Reisedurchfall und zu anderen Impfpflaster-Programmen zuzuordnen sind, hatten zum 30. September 2010 einen Buchwert von EUR 167 Mio. Im Zuge einer Wertberichtigungsanalyse auf Basis der aktuellen Studienergebnisse erwartet Intercell, alle oder einen großen Teil dieser Anlagegüter wertzuberichtigen. Diese Maßnahme wird erhebliche Auswirkungen auf den prognostizierten Verlust für das Gesamtjahr 2010 haben. Außerdem geht Intercell davon aus, weder im Jahr 2010 noch in Zukunft die bisher erwarteten Meilensteinzahlungen in Zusammenhang mit dem Programm gegen Reisedurchfall zu erhalten. Intercell hat daher beschlossen, die Ausgaben für Forschung und Entwicklung im Jahr 2011 erheblich um etwa 40 % im Vergleich zu 2010 zu reduzieren. Auch die organisatorische Struktur wird entsprechend angepasst werden. Diese Maßnahmen sollen bis Mitte 2011 vollständig umgesetzt sein und im Jahr 2012 sowie in den folgenden Jahren zu weiteren Kostensenkungen führen.
"Wir sind sehr enttäuscht über diese unerwarteten Ergebnisse der Phase II- und Phase III-Studien unseres Impfpflasters gegen Reisedurchfall. Dennoch sind wir davon überzeugt, eine klare Strategie für eine weitere gut ausgewogene Entwicklung unserer starken Pipeline zu haben. Unser Impfstoff gegen Japanische Enzephalitis ist bereits auf dem Markt und ein global führendes und sehr attraktives Portfolio zur Erforschung nosokomialer Impfstoffe befindet sich im fortgeschrittenen klinischen Entwicklungsstadium. Darüber hinaus haben wir noch einige viel versprechende präklinische Impfstoff- und Antikörper-Kandidaten", sagt Gerd Zettlmeissl, CEO von Intercell. "Unser Management hat alle nötigen Maßnahmen ergriffen, um den operativen Betrieb des Unternehmens entsprechend auszurichten."
In Anbetracht dieser unerwarteten Situation hat Intercell beschlossen, den für Mittwoch, den 15. Dezember 2010, in London geplanten R&D Day auf einen späteren Zeitpunkt zu verschieben. Die Veranstaltung wird durch eine Telefonkonferenz für Analysten ersetzt, in der die gewonnenen Daten und die strategischen Implikationen im Detail dargestellt werden.
Rückfragehinweis: Intercell AG Corporate Communications Tel. +43 1 20620-1222/-1116 communications@intercell.com
Ende der Mitteilung euro adhoc -------------------------------------------------- ------------
Emittent: Intercell AG Campus Vienna Biocenter 3 A-1030 Wien Telefon: +43 1 20620-0 begin_of_the_skype_highlighting +43 1 20620-0 end_of_the_skype_highlighting FAX: +43 1 20620-800 Email: investors@intercell.com WWW: www.intercell.com Branche: Biotechnologie ISIN: AT0000612601 Indizes: ATX Prime, ATX Börsen: Amtlicher Handel: Wien Sprache: Deutsch
ISIN AT0000612601
AXC0044 2010-12-12/23:39
© 2010 dpa-AFX
http://www.finanznachrichten.de/...toffs-gegen-reisedurchfall-016.htm
finde, ist wirklich, dass diese Aktie schon bei 30 Euro stand ohne dass ein Produkt vor 2 Jharen zugelassen war....einfach immer höher gejubelt.
Die Aufgabe dieses Pflaster gegen Durchfallerkrankungen ist schonrecht bitter; zum Glück hat Intercell noch eine gute Pipleline und kann es meines Erachtens gut verschmerzen, aber trotzdem hier ist vermutlich erst einmal ein wenig die Luft raus.
Und was richtig deftig was wert wäre, im Falle eines Erfolges: Merck in P3 mit s.aureus-Impfstoff. Das sind Multiresistene Krankenhauskeime. Das kann möglicherweise mehrere Milliarden Umsatz bei Merck bringen und 12 oder 15% Tantieme für ICLL, wenn ich recht erinnere.
http://www.intercell.com/de/main/forvaccperts/produktentwicklung/
Nach dem Absturz kann es durchaus ein Kauf sein, aber heute Mittag wollen sicher auch noch ein par Amis liquidieren....
Hallo, gerade diesen Bericht gefunden:
Intercell AG, einer der einstigen Highflyer an der Wiener Börse stürzt heute ab. Mit einem satten Minus von über 40 Prozent quittieren die Anleger des Biotechnologie Unternehmens heute die Meldung, dass einer der Hoffnungsträger des Unternehmens, ein einfach ... www.investor-sms.de/Boersenbriefe/...de/Intercell-AG-Aktie-stuerzt-ab
Quelle: http://www.investorsinside.de
lg,
paris
*INTERCELL CEO SAYS HAS "NO ISSUE" ON CASH FOR "1-2 YEARS"
*INTERCELL CEO SAYS FY LOSS COULD BE AROUND EU200 MLN
*INTERCELL CEO SAYS TO CONTINUE GLAXO COOPERATION ON PATCHES
(bloomberg)
So kommt es, wenn man eine Firma (iomai) übernimmt, und dann den goodwill wegschmeissen muss......
die Finger lassen....mit wenigen Ausnahmen.
Wer hier zuviel Geld reingebuttert hat sollte mal schauen, wie sich im Jahr 2010 Rohstoffaktien, Gold & Silber, Autotitel und Zulieferer entwickelt haben...
Meine Erfahrung mit Biotechs ist fast ausschliesslich schlecht. Intercell wird sch zwar die nächsten Wochen vielleicht wieder auf 12-14 Euro hin aufrappeln aber wenn man bedenkt, dass die schon mal bei 30 Euro standen.
Tatsache ist, dass sich das Risiko bei den wenigsten Biotechs wirklich lohnt. Selbst als Beimischung im Depot macht es leider nur wenig Sinn finde ich...man muss sich sehrt gut auskennen mit den Firmen un deren Pipeline und niemand ist gefeit gegen solche Abstütze wie heute.
und wer jetzt als ösi kauft entgeht der neuen 25% steuer
lg
BO
Natürlich sind Biotechs immer ein Risiko, aber ich glaube der Abschlag ist zu heftig.
Vielleicht liege ich aber auch völlig daneben, wir werden sehen.
Die Pipeline sieht aber doch recht vielversprechend aus und daher bin ich positiv, was die Kursentwicklung angeht, wenn der erste Schreck verflogen ist.
Impfstoff für S.aureus ist ja auch noch in der mache und der hat sicher ein ordentliches Umsatzpotential.....wenn er kommt ;-)