Celgene - Steigflug des Biostars
| eröffnet am: | 02.10.12 19:57 von: | MPower |
| neuester Beitrag: | 22.05.18 15:41 von: | iTechDachs |
| Anzahl Beiträge: | 47 | |
| Leser gesamt: | 46499 | |
| davon Heute: | 7 | |
bewertet mit 2 Sternen |
||
|
|
||
wer ist hier noch in Celgene investiert, die Firma ist ein kleiner Schatz, wächst fröhlich vor sich hin während die Normalen Anleger noch nicht auf sie aufmerksam geworden sind.
Gruesse aus Finnland
http://www.pharma-zeitung.de/...e-stellungnahme-des-chmp-fur.7124.php
(26.01.2015, Pharma-Zeitung.de) BOUDRY, Schweiz - Copyright by Business Wire - Celgene International Sàrl
In Europa ist das Bronchialkarzinom die am vierthäufigsten diagnostizierte Krebserkrankung und die häufigste Ursache für krebsbedingte Todesfälle.
Celgene International Sàrl, eine hundertprozentige Tochtergesellschaft der Celgene Corporation (NASDAQ: CELG), gab heute bekannt, dass der Ausschuss für Humanarzneimittel (Committee for Medicinal Products for Human Use; CHMP) der Europäischen Arzneimittel-Agentur (European Medicines Agency; EMA) eine positive Stellungnahme zu ABRAXANE® (Paclitaxel in einer Formulierung als albumingebundene Nanopartikel bzw. nab-Paclitaxel) in Kombination mit Carboplatin als Erstlinientherapie beim nicht-kleinzelligen Bronchialkarzinom bei erwachsenen Patienten, die für eine möglicherweise kurative chirurgische Resektion oder Strahlentherapie nicht infrage kommen, abgegeben hat.
Das Bronchialkarzinom ist die am vierthäufigsten diagnostizierte Krebserkrankung bei Männern und Frauen sowie die häufigste krebsbedingte Todesursache in Europa. Das nicht-kleinzellige Bronchialkarzinom (Non-Small Cell Lung Cancer; NSCLC) ist die häufigste Form des Bronchialkarzinoms und für 85 bis 90 Prozent aller Fälle verantwortlich. Am häufigsten wird die Erkrankung durch den Konsum von Zigaretten ausgelöst, wobei aber auch umweltbezogene und berufsbedingte Faktoren ursächlich sein können. Zu den Behandlungsoptionen gehören in der Regel systemische Chemotherapie und Proteinkinase-Inhibitoren. In sehr weit fortgeschritten Fällen ist nur noch eine symptomatische Behandlung möglich. Es besteht ein klarer Bedarf an neuen Arzneimitteln zur Behandlung des Bronchialkarzinoms.
„Fortschritte bei der Behandlung des Bronchialkarzinoms können erstens durch eine frühzeitige Diagnosestellung bei Patienten entstehen, die beim Auftreten von Symptomen umgehend einen Arzt aufsuchen, und zweitens durch neue Arzneimittel, die gut verträglich sind und die gegenwärtig eingesetzten Therapien verbessern. Angesichts der Häufigkeit und Aggressivität des Bronchialkarzinoms können kleinere Fortschritte eine große Bedeutung für Patienten und die Gesellschaft haben“, so Dr. Mary O’Brien, Consultant Medical Oncologist, The Royal Marsden NHS Foundation Trust, Großbritannien. „Die positive Stellungnahme des CHMP zu ABRAXANE in Kombination mit Carboplatin zur Behandlung erwachsener Patienten mit NSCLC ist ein wichtiger Schritt, um Patienten in Europa neue Behandlungsoptionen zu bieten. Die klinischen Daten zeigen eine signifikant positive Ansprechrate auf die Behandlung in Kombination mit einem bekannten Sicherheitsprofil. Die Behandlung führte zudem zu einem signifikanten Vorteil hinsichtlich des Ansprechens einer Untergruppe von Patienten mit Plattenepithelkarzinom der Lunge, eine Krebserkrankung, bei der in den letzten Jahren nur wenige Fortschritte erzielt wurden.”
Die positive CHMP-Stellungnahme stützt sich auf die Ergebnisse einer multizentrischen, randomisierten, offenen Studie, an der 1052 chemotherapienaive Patienten mit nicht-kleinzelligem Bronchialkarzinom im Stadium III b/IV teilnahmen. Die Studie verglich ABRAXANE in Kombination mit Carboplatin mit lösungsmittelbasiertem Paclitaxel in Kombination mit Carboplatin als Erstlinientherapie bei Patienten mit fortgeschrittenem nicht-kleinzelligem Bronchialkarzinom. Der primäre Wirksamkeitsendpunkt, die Gesamtansprechrate, lag mit 33 Prozent bei Patienten der ABRAXANE-plus-Carboplatin-Gruppe signifikant höher als bei den Patienten der Kontrollgruppe (25 Prozent). Die häufigsten unerwünschten Ereignisse, die unter der ABRAXANE-plus-Carboplatin-Kombinationstherapie bei mindestens 20 Prozent der Patienten mit NSCLC auftraten, waren Anämie, Neutropenie, Thrombozytopenie, periphere Neuropathie, Übelkeit und Fatigue.
„Die positive Stellungnahme des CHMP gibt Celgene erstmals die Gelegenheit, dazu beizutragen, Patienten mit NSCLC in Europa Zugang zu einer wichtigen Behandlungsoption zu bieten“, sagt Tuomo Pätsi, Präsident von Celgene in Europa, Nahost und Afrika (EMEA). „Die erwartete Entscheidung der Europäischen Kommission würde die dritte zugelassene Indikation für ABRAXANE darstellen, was den Wert dieses Medikaments unterstreicht. Wir werden sicherstellen, dass Patienten, die ABRAXANE benötigen, Zugang zu dieser Therapie erhalten, sobald die Zulassung durch die Europäische Kommission erfolgt ist.“
Das CHMP prüft Zulassungsanträge für alle 28 Mitgliedstaaten der Europäischen Union (EU) sowie für Norwegen, Liechtenstein und Island. Die Europäische Kommission folgt im Allgemeinen den Empfehlungen des CHMP. Mit einer endgültigen Entscheidung wird in etwa zwei Monaten gerechnet. Sollte die Zulassung erfolgen, werden die genauen Bedingungen für die Anwendung des Arzneimittels in der Zusammenfassung der Produkteigenschaften (Summary of Product Characteristics; SmPC) dargelegt, die im überarbeiteten EPAR-Bericht (European Public Assessment Report) veröffentlicht wird. Zudem wird die deutsche Fachinformation für ABRAXANE entsprechend aktualisiert.
ABRAXANE ist derzeit in der Europäischen Union nicht für die Behandlung des metastasierten nicht-kleinzelligen Bronchialkarzinoms zugelassen.
Über ABRAXANE
ABRAXANE ist eine albumingebundene Form von Paclitaxel. Es wird unter Verwendung der patentierten nab®-Technologie hergestellt. ABRAXANE enthält Albumin, ein humanes Protein, und ist frei von Lösungsmitteln.
ABRAXANE wurde erstmals im Januar 2005 von der US-amerikanischen Arzneimittelaufsichtsbehörde FDA zur Behandlung von Brustkrebs nach dem Versagen einer Kombinationschemotherapie bei Metastasen oder einem Rezidiv innerhalb von sechs Monaten nach einer adjuvanten Chemotherapie zugelassen. Sofern nicht klinisch kontraindiziert, sollte vor der Therapie ein Anthracyklin verabreicht worden sein. In Europa wurde ABRAXANE im Januar 2008 als Monotherapie zur Behandlung des metastasierten Mammakarzinoms bei erwachsenen Patienten zugelassen, bei denen die Erstlinientherapie der metastasierten Erkrankung fehlgeschlagen ist und für die eine standardmäßige Anthracyclin enthaltende Therapie nicht angezeigt ist. Weltweit wurde ABRAXANE bisher in mehr als 50 Ländern zur Behandlung des metastasierten Mammakarzinoms zugelassen.
Im Oktober 2012 wurde ABRAXANE von der US-Gesundheitsbehörde FDA als Erstlinientherapie beim lokal fortgeschrittenen oder metastasierten nicht-kleinzelligen Bronchialkarzinom (NSCLC) in Kombination mit Carboplatin bei Patienten zugelassen, die nicht für eine kurative chirurgische Resektion oder Strahlentherapie infrage kommen. ABRAXANE ist auch in Argentinien, Australien, Chile, Ecuador, Guatemala, Hongkong, Japan, Neuseeland und Singapur zur Behandlung des NSCLC zugelassen.
Im September 2013 wurde ABRAXANE von der US-Gesundheitsbehörde FDA in Kombination mit Gemcitabin als Erstlinientherapie bei Patienten mit metastasiertem Adenokarzinom des Pankreas zugelassen. Im Dezember 2013 wurde ABRAXANE in Kombination mit Gemcitabin in Europa als Erstlinientherapie bei erwachsenen Patienten mit metastasiertem Adenokarzinom des Pankreas zugelassen. Weltweit wurde ABRAXANE bisher in mehr als 40 Ländern zur Behandlung von metastasiertem Bauchspeicheldrüsenkrebs zugelassen
Aufsichtsrechtliche Informationen zu ABRAXANE für die USA
WARNUNG – NEUTROPENIE
ABRAXANE darf Patienten, deren Neutrophilenzahl zu Behandlungsbeginn unter 1500 Zellen/mm3 liegt, nicht verabreicht werden. Um das mögliche Auftreten einer Knochenmarksuppression zu überwachen, insbesondere Neutropenie, die einen schweren Verlauf nehmen und zu Infektionen führen kann, werden für alle Patienten unter ABRAXANE-Behandlung häufige Blutbildkontrollen empfohlen.
Hinweis: Eine albumingebundene Form von Paclitaxel kann die funktionellen Eigenschaften eines Wirkstoffs im Verhältnis zu denen des aufgelösten Wirkstoffs erheblich beeinträchtigen. NICHT DURCH ANDERE PACLITAXEL-FORMULIERUNGEN ERSETZEN ODER AN DEREN STELLE VERWENDEN!
GEGENANZEIGEN
Neutrophilenzahl
ABRAXANE darf Patienten, deren Neutrophilenzahl zu Behandlungsbeginn unter 1500 Zellen/mm3 liegt, nicht verabreicht werden.
Überempfindlichkeit
Patienten, bei denen schwere Überempfindlichkeitsreaktionen auf ABRAXANE festgestellt wurden, sollte das Medikament nicht erneut verabreicht werden.
WARNHINWEISE UND VORSICHTSMASSNAHMEN
Hämatologische Wirkungen
Die Knochenmarkdepression (vorwiegend Neutropenie) ist dosisabhängig und eine dosislimitierende Toxizität von ABRAXANE. In klinischen Studien wurde eine Neutropenie dritten oder vierten Grades bei 34 Prozent der Patientinnen mit metastasiertem Brustkrebs (mBC), 47 Prozent der Patienten mit nicht-kleinzelligem Bronchialkarzinom (NSCLC) und 38 Prozent der Patienten mit Bauchspeicheldrüsenkrebs festgestellt.
Beobachten Sie die Patienten auf Anzeichen von Myelotoxizität durch häufige Blutbildkontrollen – bei metastasiertem Brustkrebs (mBC) vor der Verabreichung am 1. Tag des Behandlungszyklus und bei nicht-kleinzelligem Bronchialkarzinom (NSCLC) und Bauchspeicheldrüsenkrebs an den Tagen 1, 8 und 15.
ABRAXANE sollte Patienten mit einem Ausgangswert der absoluten Neutrophilenzahl (ANC) unter 1500 Zellen/mm3 nicht verabreicht werden.
Falls im Verlauf einer ABRAXANE-Therapie eine schwere Neutropenie (weniger als 500 Zellen/mm3 über sieben Tage oder länger) auftritt, ist die ABRAXANE-Dosis bei Patienten mit mBC oder NSCLC für die weitere Behandlung zu verringern.
Bei Patientinnen mit mBC ist die Behandlung mit dreiwöchentlichen Verabreichungszyklen von ABRAXANE fortzusetzen, nachdem ihre absolute Neutrophilenzahl wieder auf über 1500 Zellen/mm3 und ihre Thrombozytenzahl wieder auf über 100.000 Zellen/mm3 angestiegen sind.
Bei NSCLC-Patienten ist die Behandlung, falls ärztlich empfohlen, mit permanent reduzierten Dosierungen der wöchentlichen Verabreichung von ABRAXANE und der dreiwöchentlichen Verabreichung von Carboplatin fortzusetzen, sobald am 1. Tag des Behandlungszyklus eine absolute Neutrophilenzahl von mindestens 1500 Zellen/mm3 und eine Thrombozytenzahl von mindestens 100.000 Zellen/mm3 oder am 8. oder 15. Tag des Behandlungszyklus eine absolute Neutrophilenzahl von mindestens 500 Zellen/mm3 und eine Thrombozytenzahl von mindestens 50.000 Zellen/mm3 erreicht wird.
Bei Patienten mit einem Adenokarzinom des Pankreas sind ABRAXANE und Gemcitabin abzusetzen, falls die absolute Neutrophilenzahl weniger als 500 Zellen/mm3 oder die Thrombozytenzahl weniger als 50.000 Zellen/mm3 beträgt. Der Beginn des nächsten Behandlungszyklus sollte aufgeschoben werden, falls die absolute Neutrophilenzahl am 1. Tag des Behandlungszyklus unter 1500 Zellen/mm3 oder die Thrombozytenzahl unter 100.000 Zellen/mm3 liegt. Falls empfohlen, wird die Behandlung mit einer entsprechend reduzierten Dosis fortgesetzt.
Nervensystem
Das Risiko einer sensorischen Neuropathie ist dosis- und schemaabhängig.
Das Auftreten einer sensorischen Neuropathie ersten oder zweiten Grades erfordert im Allgemeinen keine Änderung der Dosierung.
Im Fall einer sensorischen Neuropathie dritten oder höheren Grades sollte die Behandlung von mBC-Patientinnen bis zum Abklingen auf den ersten oder zweiten Grad bzw. die Behandlung von Patienten mit NSCLC oder Bauchspeicheldrüsenkrebs bis zum Abklingen auf den ersten Grad oder vollständigen Abklingen unterbrochen werden. Im Anschluss sollte eine Dosisreduktion für alle nachfolgenden ABRAXANE-Behandlungen erfolgen.
Sepsis
Bei fünf Prozent der Patienten mit oder ohne Neutropenie, die ABRAXANE in Verbindung mit Gemcitabin erhielten, trat eine Sepsis auf.
Ein Verschluss der Gallenwege oder das Vorhandensein eines biliären Stents waren Faktoren, die das Risiko einer schweren oder tödlichen Sepsis beeinflussten.
Falls ein Patient febril wird (unabhängig von der absoluten Neutrophilenzahl) ist eine Behandlung mit einem Breitspektrumantibiotikum einzuleiten.
Im Falle einer febrilen Neutropenie ist die Behandlung mit ABRAXANE und Gemcitabin zu unterbrechen, bis sich das Fieber legt und die absolute Neutrophilenzahl bei mindestens 1500 Zellen/mm3 liegt. Anschließend kann die Behandlung mit einem niedrigeren Dosierungsniveau fortgesetzt werden.
Pneumonitis
Pneumonitis, einschließlich einiger Fälle mit tödlichem Ausgang, trat bei vier Prozent der Patienten auf, die ABRAXANE in Kombination mit Gemcitabin erhielten.
Überwachen Sie die Patienten auf Symptome der Erkrankung und unterbrechen Sie die Verabreichung von ABRAXANE und Gemcitabin, wenn ein Verdacht auf Pneumonitis besteht.
Wird eine Pneumonitis diagnostiziert, sind ABRAXANE und Gemcitabin dauerhaft abzusetzen.
Überempfindlichkeit
Es wurden Fälle von schweren und manchmal tödlich verlaufenden Überempfindlichkeitsreaktionen berichtet, einschließlich anaphylaktischer Reaktionen.
Patienten, bei denen schwere Überempfindlichkeitsreaktionen auf ABRAXANE festgestellt wurden, sollte das Medikament nicht erneut verabreicht werden.
Leberfunktionsstörungen
Da die Exposition gegenüber und Toxizität von Paclitaxel bei Leberfunktionsstörungen erhöht sein kann, ist bei der ABRAXANE-Behandlung von Patienten mit Leberfunktionsstörungen besondere Vorsicht geboten.
Bei Patienten mit eingeschränkter Leberfunktion besteht möglicherweise ein erhöhtes Toxizitätsrisiko, insbesondere durch Myelosuppression. Überwachen Sie die Patienten auf Anzeichen einer schweren Myelosuppression.
Bei der Behandlung von mBC und NSCLC sollten Patienten mit mittelschweren bis schweren Leberfunktionsstörungen eine niedrigere Anfangsdosis erhalten.
Bei der Behandlung von Adenokarzinomen des Pankreas wird ABRAXANE nicht für Patienten mit mittelschweren bis schweren Leberfunktionsstörungen (mit einem Gesamt-Bilirubin von mehr als dem 1,5-fachen der oberen Normgrenze und einer AST von mehr als dem 10-fachen der oberen Normgrenze) empfohlen.
Humanalbumin
ABRAXANE enthält Humanalbumin, das aus menschlichem Blut gewonnen wird.
Anwendung während der Schwangerschaft: Schwangerschaftskategorie D
Eine Anwendung von ABRAXANE während der Schwangerschaft kann Schädigungen des Ungeborenen auslösen.
Bei einer Verabreichung dieses Medikaments während einer Schwangerschaft, oder wenn die Patientin während der Behandlung schwanger wird, muss sie über die Risiken für das Ungeborene aufgeklärt werden.
Frauen im gebärfähigen Alter muss nachdrücklich angeraten werden, während der Behandlung mit ABRAXANE eine Schwangerschaft zu verhüten.
Anwendung bei Männern
Männern ist davon abzuraten, während der Behandlung mit ABRAXANE ein Kind zu zeugen.
NEBENWIRKUNGEN
Randomisierte Studie an Patientinnen mit metastasiertem Brustkrebs (mBC)
Die häufigsten Nebenwirkungen, die während der mBC-Studie unter einer Monotherapie mit ABRAXANE bei mindestens 20 Prozent der Patienten auftraten, waren (verglichen mit Paclitaxel-Injektionen) Alopezie (90 vs. 94 Prozent), Neutropenie (alle Fälle 80 vs. 82 Prozent, schwere Fälle 9 vs. 22 Prozent), sensorische Neuropathie (alle Symptome 71 vs. 56 Prozent, schwere Fälle 10 vs. 2 Prozent), pathologische EKG-Veränderungen (alle Patienten 60 vs. 52 Prozent, Patienten mit normalem Ausgangs-EKG 35 vs. 30 Prozent), Fatigue/Asthenie (alle 47 vs. 39 Prozent, schwere Fälle 8 vs. 3 Prozent), Myalgie/Arthralgie (alle 44 vs. 49 Prozent, schwere Fälle 8 vs. 4 Prozent), erhöhte AST-Werte (alle 39 vs. 32 Prozent), erhöhte alkalische Phosphatase (alle 36 vs. 31 Prozent), Anämie (alle 33 vs. 25 Prozent, schwere Fälle 1 vs. < 1 Prozent), Übelkeit (alle 30 vs. 22 Prozent, schwere Fälle 3 vs. < 1 Prozent), Diarrhö (alle 27 vs. 15 Prozent, schwere Fälle < 1 vs. 1 Prozent) und Infektionen (24 vs. 20 Prozent).
Eine sensorische Neuropathie war bei 7 von 229 (3 Prozent) Patienten der Grund des Absetzens von ABRAXANE.
Sonstige nennenswerte Nebenwirkungen durch die Anwendung von ABRAXANE im Vergleich zur Paclitaxel-Injektion waren Erbrechen (alle 18 vs. 10 Prozent, schwere Fälle 4 vs. 1 Prozent), Flüssigkeitseinlagerung (alle 10 vs. 8 Prozent, schwere Fälle 0 vs. < 1 Prozent), Schleimhautentzündungen (alle 7 vs. 6 Prozent, schwere Fälle < 1 vs. 0 Prozent), Leberfunktionsstörung (erhöhte Bilirubinwerte 7 vs. 7 Prozent), Überempfindlichkeitsreaktionen (alle 4 vs. 12 Prozent, schwere Fälle 0 vs. 2 Prozent), Thrombozytopenie (alle 2 vs. 3 Prozent, schwere Fälle < 1 vs. < 1 Prozent), neutropenische Sepsis (< 1 vs. < 1 Prozent) und Reaktionen am Injektionsort (< 1vs. 1 Prozent). Fälle von Dehydratation und Fieber wurden ebenfalls berichtet.
Nierenfunktionsstörungen (alle 11 Prozent, schwere Fälle 1 Prozent) wurden bei mit ABRAXANE behandelten Patienten (n = 229) beobachtet.
Bei allen mit ABRAXANE behandelten Patienten (n = 366) wurden Augenbeschwerden/Sehstörungen berichtet (alle 13 Prozent, schwere Fälle 1 Prozent)
Bei etwa 3 Prozent der Patienten traten schwere kardiovaskuläre Ereignisse in möglichem Zusammenhang mit der ABRAXANE-Monotherapie auf, darunter kardiale Ischämie/Herzinfarkt, Brustschmerzen, Herzstillstand, supraventrikuläre Tachykardie, Ödeme, Thrombosen, venöse Thromboembolie Lungenembolie und Hypertonie.
Ferner wurden Fälle von apoplektischem Insult (Schlaganfall) und transitorischen ischämischen Attacken (TIA) berichtet
Studie an Patienten mit nicht-kleinzelligem Bronchialkarzinom (NSCLC)
Die häufigsten unerwünschten Ereignisse, die unter der ABRAXANE-plus-Carboplatin-Kombinationstherapie bei mindestens 20 Prozent der Patienten mit NSCLC auftraten, waren Anämie, Neutropenie, Thrombozytopenie, Alopezie, periphere Neuropathie, Übelkeit und Müdigkeit.
Die häufigsten schweren Nebenwirkungen der Kombinationstherapie mit ABRAXANE und Carboplatin bei NSCLC waren Anämie (4 Prozent) und Pneumonie (3 Prozent).
Die häufigsten Nebenwirkungen, die zum dauerhaften Absetzen von ABRAXANE führten, waren Neutropenie (3 Prozent), Thrombozytopenie (3 Prozent) und periphere Neuropathie (1 Prozent).
Die häufigsten Nebenwirkungen, die zur Reduktion der ABRAXANE-Dosis führten, waren Neutropenie (24 Prozent), Thrombozytopenie (13 Prozent) und Anämie (6 Prozent).
Die häufigsten Nebenwirkungen, die eine Unterbrechung oder Verzögerung der Verabreichung von ABRAXANE zur Folge hatten, waren Neutropenie (41 Prozent), Thrombozytopenie (30 Prozent) und Anämie (16 Prozent).
Folgende häufige Nebenwirkungen wurden mit vergleichbarer Häufigkeit bei mindestens zehn Prozent der Patienten beobachtet, die mit ABRAXANE plus Carboplatin oder Paclitaxel-Injektionen plus Carboplatin behandelt wurden: Alopezie (56 Prozent), Übelkeit (27 Prozent), Fatigue (25 Prozent), verminderter Appetit (17 Prozent), Asthenie (16 Prozent), Obstipation (16 Prozent), Diarrhö (15 Prozent), Erbrechen (12 Prozent), Atemnot (12 Prozent) und Hautausschlag (10 Prozent). Die Inzidenzraten beziehen sich auf die Behandlungsgruppe ABRAXANE plus Carboplatin.
Nebenwirkungen mindestens dritten Grades mit einem Häufigkeitsunterschied von ≥ 2 Prozent, die bei der Kombinationstherapie mit ABRAXANE und Carboplatin verglichen mit der Kombinationstherapie mit Paclitaxel-Injektionen und Carboplatin zur Behandlung von NSCLC auftraten, waren Anämie (28 vs. 7 Prozent), Neutropenie (47 vs. 58 Prozent), Thrombozytopenie (18 vs. 9 Prozent) und periphere Neuropathie (3 vs. 12 Prozent).
Nebenwirkungen ersten bis vierten Grades mit einem Häufigkeitsunterschied von ≥ 5 Prozent, die bei der Kombinationstherapie mit ABRAXANE und Carboplatin im Vergleich zu einer Kombinationstherapie mit Paclitaxel-Injektionen und Carboplatin zur Behandlung von NSCLC auftraten, waren Anämie (98 vs. 91 Prozent), Thrombozytopenie (68 vs. 55 Prozent), periphere Neuropathie (48 vs. 64 Prozent), periphere Ödeme (10 vs. 4 Prozent), Nasenbluten (7 vs. 2 Prozent), Gelenkschmerzen (13 vs. 25 Prozent) und Myalgie (10 vs. 19 Prozent).
Eine Neutropenie (alle Schweregrade) wurde bei 85 Prozent der mit ABRAXANE und Carboplatin behandelten Patienten im Vergleich zu 83 Prozent der mit Paclitaxel-Injektionen und Carboplatin behandelten Patienten festgestellt.
Studie an Patienten mit Adenokarzinom des Pankreas
Von den häufigsten in der Phase-III-Studie beobachteten Nebenwirkungen, die bei mindestens 20 Prozent der Patienten unter der Kombinationstherapie mit ABRAXANE plus Gemcitabin auftraten, war die Häufigkeit der folgenden in der ABRAXANE-plus-Gemcitabin-Gruppe ≥ 5 Prozent höher als in der Gemcitabin-Gruppe: Neutropenie (73 vs. 58 Prozent), Fatigue (59 vs. 46 Prozent), periphere Neuropathie (54 vs. 13 Prozent), Übelkeit (54 vs. 48 Prozent), Alopezie (50 vs. 5 Prozent), periphere Ödeme (46 vs. 30 Prozent), Diarrhö (44 vs. 24 Prozent), Fieber (41 vs. 28 Prozent), Erbrechen (36 vs. 28 Prozent), Appetitverlust (36 vs. 26 Prozent), Ausschlag (30 vs. 11 Prozent) und Dehydratation (21 vs.11 Prozent).
Von diesen häufigsten Nebenwirkungen war die Häufigkeit einer Toxizität dritten bis vierten Grades bei den folgenden in der ABRAXANE-plus-Gemcitabin-Gruppe um mindestens 2 Prozent höher als in der Gemcitabin-Gruppe: Neutropenie (38 vs. 27 Prozent), Fatigue (18 vs. 9 Prozent), periphere Neuropathie (17 vs. 1 Prozent), Übelkeit (6 vs. 3 Prozent), Diarrhö (6 vs. 1 Prozent), Fieber (3 vs. 1 Prozent), Erbrechen (6 vs. 4 Prozent), Appetitverlust (5 vs. 2 Prozent) und Dehydratation (7 vs. 2 Prozent).
Eine Thrombozytopenie (aller Schweregrade) wurde bei 74 Prozent der Patienten in der ABRAXANE-plus-Gemcitabin-Gruppe festgestellt, verglichen mit 70 Prozent der Patienten in der Gemcitabin-Gruppe.
Die häufigsten schweren Nebenwirkungen von ABRAXANE (mit einer um ≥ 1 Prozent höheren Häufigkeit) waren Fieber (6 Prozent), Dehydratation (5 Prozent), Lungenentzündung (4 Prozent) und Erbrechen (4 Prozent).
Die häufigsten Nebenwirkungen, die zum dauerhaften Absetzen von ABRAXANE führten, waren periphere Neutropenie (8 Prozent), Fatigue (4 Prozent) und Thrombozytopenie (2 Prozent).
Die häufigsten Nebenwirkungen, die zur Reduktion der ABRAXANE-Dosis führten, waren Neutropenie (10 Prozent) und periphere Neuropathie (6 Prozent).
Die häufigsten Nebenwirkungen, die eine Unterbrechung oder Verzögerung der Verabreichung von ABRAXANE zur Folge hatten, waren Neutropenie (16 Prozent), Thrombozytopenie (12 Prozent), Fatigue (8 Prozent), periphere Neuropathie (15 Prozent), Anämie (5 Prozent) und Diarrhö (5 Prozent).
Weitere ausgewählte Nebenwirkungen aller Toxizitätsgrade, deren Häufigkeit in der ABRAXANE-plus-Gemcitabin-Gruppe ≥ 5 Prozent höher war als in der Gemcitabin-Gruppe, waren Asthenie (19 vs. 13 Prozent), Mukositis (10 vs. 4 Prozent), Dysgeusie (16 vs. 8 Prozent), Kopfschmerzen (14 vs. 9 Prozent), Hypokaliämie (12 vs. 7 Prozent), Husten (17 vs. 7 Prozent), Nasenbluten (15 vs. 3 Prozent), Harnwegsinfektionen (11 vs. 5 Prozent), Schmerzen in Extremitäten (11 vs. 6 Prozent), Gelenkschmerzen (11 vs. 3 Prozent), Myalgie (10 vs. 4 Prozent) und Depression (12 vs. 6 Prozent).
Weitere ausgewählte Nebenwirkungen der Toxizitätsgrade 3 bis 4, deren Häufigkeit in der ABRAXANE-plus-Gemcitabin-Gruppe ≥ 2 Prozent höher war als in der Gemcitabin-Gruppe, waren Thrombozytopenie (13 vs. 9 Prozent), Asthenie (7 vs. 4 Prozent) und Hypokaliämie (4 vs. 1 Prozent).
Praxiserfahrungen mit ABRAXANE und anderen Paclitaxel-Formulierungen nach Markteinführung
Im Zusammenhang mit ABRAXANE wurden schwere und manchmal tödlich verlaufende Überempfindlichkeitsreaktionen berichtet. Die Anwendung von ABRAXANE bei Patienten, bei denen zuvor Überempfindlichkeitsreaktionen gegenüber Paclitaxel-Injektionen oder Humanalbumin auftraten, wurde nicht untersucht.
Während der ABRAXANE-Behandlung wurden Fälle von Stauungsinsuffizienz, linksventrikulärer Dysfunktion und AV-Block beobachtet, insbesondere bei Patienten mit einer kardialen Grunderkrankung in der Vorgeschichte oder bei vorheriger Exposition gegenüber kardiotoxischen Wirkstoffen.
Es wurden Fälle einer Extravasation von ABRAXANE berichtet. Aufgrund der Möglichkeit einer Extravasation wird empfohlen, die ABRAXANE-Infusionsstelle engmaschig auf eine mögliche Infiltration während der Verabreichung des Medikaments zu überwachen.
WECHSELWIRKUNGEN MIT ANDEREN ARZNEIMITTELN
Bei der gleichzeitigen Verabreichung von ABRAXANE und anderen Mitteln, die CYP2C8 oder CYP3A4 hemmen oder induzieren, ist Vorsicht geboten.
ANWENDUNG BEI SPEZIELLEN PATIENTENGRUPPEN
Stillzeit
Es ist nicht bekannt, ob Paclitaxel über die Muttermilch ausgeschieden wird. Da viele Wirkstoffe über die Muttermilch ausgeschieden werden und das Risiko schwerer Nebenwirkungen bei gestillten Säuglingen besteht, ist entweder das Absetzen des Arzneimittels oder das Abstillen in Betracht zu ziehen, wobei die Bedeutung des Arzneimittels für die Mutter zu berücksichtigen ist.
Kinder und Jugendliche
Die Wirksamkeit und Sicherheit von ABRAXANE bei Kindern und Jugendlichen wurden nicht untersucht.
Ältere Patienten
Keine der Toxizitäten war bei Patientinnen im Alter von ≥ 65 Jahren, die ABRAXANE zur Behandlung von mBC erhielten, eindeutig häufiger zu beobachten.
Myelosuppression, periphere Neuropathie und Gelenkschmerzen traten häufiger bei Patienten im Alter von ≥ 65 Jahren auf, die ABRAXANE und Carboplatin zur Behandlung von NSCLC erhielten.
Bei der Behandlung des Adenokarzinoms des Pankreas mit ABRAXANE und Gemcitabin traten Diarrhö, Appetitverlust, Dehydratation und Nasenbluten bei Patienten im Alter von ≥ 65 Jahren häufiger auf als bei Patienten < 65 Jahren.
Nierenfunktionsstörungen
Die vorliegenden Daten reichen nicht aus, um Dosisempfehlungen bei Patienten mit stark eingeschränkter Nierenfunktion oder terminaler Niereninsuffizienz (geschätzte Kreatinin-Clearance < 30 ml/min) auszusprechen.
DOSIERUNG UND ART DER ANWENDUNG
ABRAXANE darf nicht an Patienten mit einem Gesamt-Bilirubin von mehr als dem 1,5-fachen der oberen Normgrenze und einer AST von mehr als dem 10-fachen der oberen Normgrenze verabreicht werden.
Bei der Behandlung von mBC und NSCLC sollten Patienten mit mittelschweren bis schweren Leberfunktionsstörungen eine niedrigere Anfangsdosis erhalten.
Bei der Behandlung des Adenokarzinoms des Pankreas sollten Patienten mit mittelschweren bis schweren Leberfunktionsstörungen kein ABRAXANE erhalten.
Dosisreduktionen oder das Absetzen der Behandlung können beim Auftreten schwerer hämatologischer, neurologischer, kutaner oder gastrointestinaler Toxizitäten erforderlich sein.
Eine engmaschige Überwachung der Patienten ist notwendig.
Bitte beachten Sie die vollständigen Verschreibungsinformationen einschließlich der gerahmten WARNHINWEISE.
Über Celgene
Celgene International Sàrl mit Sitz in Boudry im Schweizer Kanton Neuenburg ist eine hundertprozentige Tochtergesellschaft und internationaler Hauptsitz der Celgene Corporation. Die Celgene Corporation hat ihren Hauptgeschäftssitz in Summit, New Jersey, und ist ein integriertes weltweit tätiges biopharmazeutisches Unternehmen, das sich hauptsächlich mit der Erforschung, Entwicklung und Vermarktung innovativer Therapien für die Behandlung von Krebs und Entzündungskrankheiten durch Gen- und Proteinregulierung befasst. Weitere Informationen finden Sie auf der Website des Unternehmens unter www.celgene.com. Folgen Sie Celgene auf sozialen Medien: @Celgene, Pinterest, LinkedIn und YouTube.
Celgene wird am Freitag in den S$P aufgenommen. bekannt seit letztem Freitag nach Börsenschluss.
Auch hier müssen sich jetzt diverse Fonds eindecken.
Seit Freitag haben wir eine schön Aufwärtsdynamik entwickelt.
Diese mal könnte es klappen und wir schliessen die Konsolidierung seit Anfang des Jahres ab.
Auch hier haben wir ein aufsteigendes Dreieck im CHart.
sollten die 125$ wiederstände genommen werden sollten wir zügig
Richtung 130$ laufen.
Celgene hat nach Börsenschluss gute news herrausgegeben:
Phase II Data for Celgene’s Investigational Oral GED-0301 for Patients with Active Crohn’s Disease Published in New England Journal of Medicine
hier mehr dazu:
http://finance.yahoo.com/news/phase-ii-data-celgene-investigational-210500515.html
http://blogs.barrons.com/stockstowatchtoday/2015/...ories-in-biotech/
Die Ratings des Unternehmens lauten wie folgt:
2 x strong buy
17 x buy
4 x outperform
2 x hold
1 x sell
Quelle: http://www.marketbeat.com/stocks/NASDAQ/CELG/?MostRecent=1
22 der Ratings auf dieser Seite sind aus 2015 - hier werden stets die aktuellen Ratings eingestellt. Auf finanzen.net findet man ja leider nur 5 Ratings aus 2015 (siehe: http://www.finanzen.net/analysen/Celgene-Analysen) - darunter buy Ratings von UBS (das neueste vom 06.11.2015), die auf der Marketbeat Seite nicht eingestellt sind.
Wird der Bereich um die 100$ getestet und hält Stand, wäre das für mich ein positives Signal und ich würde ein erstes Investment tätigen.
Wie sind hier die Meinungen der anderen User ?
Aktienanalyst Brian Abrahams vom Investmenthaus Jefferies & Co bekräftigt laut einer aktuellen Aktienanalyse seine Kaufempfehlung für die Aktien des US-Biotechunternehmens Celgene Corp. (ISIN: US1510201049, WKN: 881244, Ticker-Symbol: CG3, Nasdaq-Symbol: CELG).
Ein Gespräch mit dem Chef der Abteilung Forschung & Entwicklung habe insgesamt einen positiven Eindruck hinterlassen. Es herrsche Optimismus, dass Celgene Corp. mehrere hochqualitative Kandidaten in frühen Entwicklungsstadien habe. Die meisten dieser potenziellen Medikamente seien noch nicht in den Konsensprognosen berücksichtigt.
Die Analysten von Jefferies & Co sind der Meinung, dass das Vertrauen in Celgene's Fähigkeit steigen könnte, auch nach dem Auslaufen des Revlimid-Patentschutzes bedeutende Umsätze zu generieren und höhere Aktienkurse zu erreichen.
Die Aktienanalysten von Jefferies & Co halten in ihrer Celgene-Aktienanalyse am Votum "buy" fest und bestätigen das Kursziel von 141,00 USD.
Quelle: http://www.aktiencheck.de/exklusiv/...Qualitaet_Aktienanalyse-6883201
http://www.nasdaq.com/article/...vlimid-patent-dispute-20151222-00732
Ich wünsche allen ein schönes entspanntes Weihnachtsfest und einen guten Rutsch ins neue Jahr, in dem man wohl an Celgene noch viel Freude haben wird :-)
Beste Grüße
Lauerte
solange der NASDAQ Biotechnologie - Index schwächelt
https://www.onvista.de/index/chart/NASDAQ-BIOTECHNOLOGY-Index-2569917
und Celgene im Abwärtstrend läuft: Charttechnisches Kaufsignal abwarten
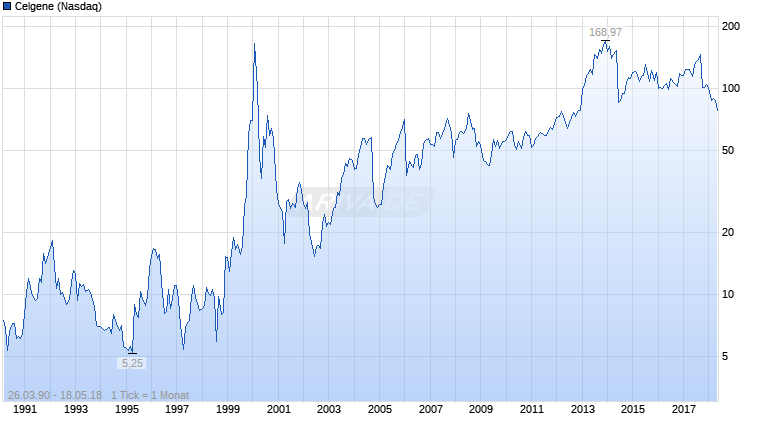
https://www.onvista.de/index/chart/NASDAQ-BIOTECHNOLOGY-Index-2569917


